La adrenalina induce adenilato ciclasa y esta AMPc que activa la fosforilaza que activa una fosforilasa que actua en al glucogenofosforilasa y degrada el glucógeno a glucosa 1 fosfato y luego a glucosa 6 fosfato y luego a glucosa.
Si la quinasa activa la glucógenosintasa, que se INACTIVA y se inhibe la sintesis de glucógeno.
Adrenalina--adenilato ciclasa--AMPc---proteína quinasa---fosforilasa---glucógenosfosforilasa
Adrenalina--adenilato ciclasa--AMPc---proteina quinasa---fosforilasa--glucógenosintasa---INHIBE SÍNTESIS DE GLUCÓGENO.
jueves, 24 de enero de 2013
Sistema de señalización por secreción de adrenalina
La adrenalina llega al receptor de membrana, se produce un cambio conformacional y la síntesis de GTP, lo que produce la activación de la subunidad alfa, la creación de adenilato ciclasa, de AMPc. La proteína quinasa A está formada por:
* dos unidades a las que se unen dos AMPc por unidad.
*dos unidades catalíticas que se activan cuando el AMPc activa las subunidades reguladoras.
Las subunidades catalíticas se unen a la CREB (proteín de unión al elemento de respuesta del AMPc,que es un factor de transcripción que se activa con la dimerización de la CREB (UNIÓN DE DOS CREB) para la formación de más proteína CREB.
El chute de adrenalina o glucagón actúa en el organismo produciendo la degradación de glúcidos.
* dos unidades a las que se unen dos AMPc por unidad.
*dos unidades catalíticas que se activan cuando el AMPc activa las subunidades reguladoras.
Las subunidades catalíticas se unen a la CREB (proteín de unión al elemento de respuesta del AMPc,que es un factor de transcripción que se activa con la dimerización de la CREB (UNIÓN DE DOS CREB) para la formación de más proteína CREB.
El chute de adrenalina o glucagón actúa en el organismo produciendo la degradación de glúcidos.
Desensibilación
La señalización por parte de la molécula señal debe ser limitada, por lo que la desensibilación impide que la proteina G se active ante la señal. La quinasa del receptor de la proteína G permite la fosforliación de los dominios citosólicos de la proteina G por lo que la arrestina puede actuar e impedir que la señal active la proteína G.
Por otr parte, la arrestine permite que los receptores abandonen la membrana gracias a que la arrestina funcionará como proteína adaptadora para la Ap2 y se forme una vesícula endocítica. Las caveolinas son un tipo específico de vesícula endocítica y se producen especialmetne en la zona de las balsas o rafts de la membrana.
Enfermedades por desensibilación:
Deshidratación: La toxina botulínica bloquea la actividad GTP, asi que la proteína está siempre activa y se produce siempre adenilciclasa y GMPc, lo que en el intestino provoca la perdida de H2O.
Señalización
ÁCIDO NÍTRICO Y CO
Las células endoteliales de lso vasos sanguíneos están enervadas por terminaciones productoras de acetilcolina. Cuando la acetilcolina llega a las células endoteliales se produce la apertura de canales de Ca y aumenta la concentración de Ca en el citosol, lo que activa ciertas proteínas.
La calmodulina es una de ellas,la calmodulina a su vez activa la oxidoniticosintasa, qeu convierte la argenina en citrulina, liberando NO. Este NO cuando llega al músculo liso de los vasos sanguíneos activa la guanilato ciclasa y se produce GMPc, que secuestra Ca y hace que se relaje el vaso sanguíneo, por lo que aumenta su area, y disminuye la presión.
Aplicaciones médicas:
**Angina de pecho. Una pastilla de nitroglicerina se coloca en la boca. Cuando se digiere produce en NO, lo que provoca la activación de la guanilato ciclasa.
**Viagra: Evita la degradación del GMPc, con lo que se secuestra Ca y e disminue la presión
Receptores de las células diana
*Receptores de canales iónicos: Recordar la liberación de acetilcolina que regula los canales de Na en células musculares.
*Receptores unidos a proteína G. La proteina G es una proteína transmembrana multimerica que atraviesa la membrana hasta en tres ocasiones y está formada por tres subunidades. La subunidad alfa presenta un dominio de unión al GTP. Cuando esta subunidad se activa, se disocian beta y gamma y se producen distintos procesos.
Estudio profundo de los receptores unidos a proteína G:
En la córnea la molécula señal es la rodopsina y el receptor se activa por luz.
¿Cómo funcionan estos receptores?
La molécula señal llega al receptor e induce un cambio conformacional, que produce el acoplamiento de la subunidad alfa con la proteina G. La subunidad alfa activará la adenilato ciclasa y se fabricará AMPc (mensajero secundario). Esta actividad GTPasica está regulada por la RDS (proteína reguladora de la señalización de la proteína G).
Receptores de las células diana
En las células diana hay tres tipos de recpetores distintos:
*Receptores de canales ionicos: Liberan acetilcolina que regula los canales de Na en las células musculares.
*Receptores unidos a la proteína G. La proteína G es una proteína multimérica qeu atraviesa la membrana hasta en 7 ocasiones. Presenta un dominio de unión al GTP. Cuando esta activada, se disocian sus subunides gamma y beta, lo que provoca distintas situaciones.
*Receptores con actividad catalítica: Tienen act. catalítica, enzimática o están unidos a proteínas citosólicas que presentan dicha actividad.
Estudio profundo de los recpetores de mebrana asociados a proteína G:
En el caso de la retina, la proteína G es la rodopsina y el receptor se activa por la luz.
¿Cómo se produce la activación genérica en esta vía de señalización?
Cuando llega la molécula señal (ej; adrenalina, rodopsina) se une al receptor y mediante los bucles citosólicos de la p. transmembrana se produce un cambio de conformación que produce el acoplamiento de la proteína G con la subunidad alfa. Una vez se disocian las unidades de la proteína G la subunidad alfa se dirigirá a la adenilato ciclasa para formar AMPc, y se produce una serie de reacciones. Cuando se hidroliza el GTP, se inactiva el AMPc. Esta actividad GTPásica está regulada por la RGS (proteína reguladora de la señalización de la proteína G)
Ácido nítrico y CO
Las células endoteliales de los vasos sanguíneos están enervadas por terminaciones que fabrican acetilcolina. Cuando la acetilcolina llega a las células endoteliales, se abren los canales de Ca2+ y aumenta la concentración de Ca2+ en el citosol. Esto provoca la activación de una serie de proteínas.
La calmodulina es activada y hace que actúe la oxidonítricosintasa que convierte la argenina en citrulina, liberando NO. Este NO cuando llega a las células musculares lisas de la pared del vaso sanguíneo activa la guanilato ciclasa, que induce la formación de GMPc, que secuestra Ca2+ y provoca la relajación del vaso sanguíneo, lo que aumenta el área de este y disminuye la presión.
Aplicaciones médicas:
*Cuando hay una angina de pecho se coloca una pastilla de nitroglicerina en la boca, que al descomponerse libera NO y se reduce la presión.
*La viagra usa este sistema y evita que se degrade el GMPc para que pueda seguir secuestrando Ca2+ y haya flujo sanguíneo.
Proteínas mitóticas motoras
Quinesinas mitóticas: Segregan los centrosomas en la anafase B mediante alargamiento de los microtúbulos polares y del áster. Además se encargan del deslizamiento hacia el extremo +.
Dineias mitóticas: Deslizamiento hacia el extremo -.
miércoles, 23 de enero de 2013
Repaso Cáncer I
El cáncer tiene un origen común: se debe a una falta de regulación del ciclo celular y además es un proceso que aunque produce daños importantes en las células, generalmente estas sobreviven.
Se pueden dar varias situaciones:
Qu se expresen proteínas no correspondientes a la fase celular.
Que una proliferación excesiva se extienda por el organismo y de lugar a un tumor maligno.
Que se facilite la liberación de factores de crecimiento para lograr la angiogénesis, ya que aunque las células tumorales no necesitan oxígeno, si necesitan nutrientes.
El cáncer es una enfermedad genética ya que se debe a un daño en el ADN, no obstante no es una enfermedad hereditaria a no ser que se transmita a través de los gamétos.
Características de las células tumorales.
1. Omiten la apoptosis.
2. Liberan factores de crecimiento por vía endocrina o paracrina.
3. Inducen la angiogénesis.
4. No necesitan oxígeno, pero sí nutrientes.
5. Carecen de capacidad de diferenciación.
6. Se extienden por el organismo mediante metástasis.
Fuente del cáncer.
Agentes químico:
Nitritos, nitrosaminas, benzopirenos, emtales pesados como Pb o Hg. Percival Plott detectó un tipo específico de cáncer en desollinadores debido a un componente químico del hollín.
Agentes físicos.
Radiaciones ionizantes, cósmicas o UVA.
Agentes biológicas:
Virus del papiloma humano. Helicobactter pylori.
Diferencia entre tumoración maligna y beningna.
Núcleo t. benigna: Pequeño
Núcleo t. maligna: Grande
Bordes nucleares: Regulares
Bordes nucleares: Irregulares
Relación núcleo/citoplasma de la t. benigna: Bajo
Relación núcleo/citoplasma de la t. maligna: Alta
Bordes tumorales de la t. benigna: Regulares
Bordes tumorales de la t. maligna: Irregulares
Organización tisular: Normal
Organizacón tisular:Desordenada
índice mitótico de la t. benigna: Bajo
Índice mitótico de la t.maligna: Alto
Diferenciación de la t. benigna: Alta
Diferencición de la t.maligna: Indeferenciada
7 diferencias entre tumoración maligna y benigna
Tamaño núcleo de la t benigna: Pequeño
Tamaño núcleo de la t. maligna: Grande
Relación núcleo/citoplasma de la t.benigna: Baja
Relación núcleo/citoplasma de la t.maligna: Alta
Índice mitótico de la t. benigna: Bajo
Índice mitótico de la t. maligna: Alto
Diferenciación de la t. benigna: Muy diferenciada
Diferenciación de la t. maligna: Indiferenciadas-
Bordes tumorales de la t. benigna: Regulares
Bordes tumorales de la t. maligna: Irregulares
Contorno nuclear de la t- benigna: Normal
Contorno nuclear de la t. maligna: Irregular
Organización tisular de la t. benigna:Organizada
Organización tisular de la t. maligna: Desorganizada
Tamaño núcleo de la t. maligna: Grande
Relación núcleo/citoplasma de la t.benigna: Baja
Relación núcleo/citoplasma de la t.maligna: Alta
Índice mitótico de la t. benigna: Bajo
Índice mitótico de la t. maligna: Alto
Diferenciación de la t. benigna: Muy diferenciada
Diferenciación de la t. maligna: Indiferenciadas-
Bordes tumorales de la t. benigna: Regulares
Bordes tumorales de la t. maligna: Irregulares
Contorno nuclear de la t- benigna: Normal
Contorno nuclear de la t. maligna: Irregular
Organización tisular de la t. benigna:Organizada
Organización tisular de la t. maligna: Desorganizada
Causas del cáncer
Agentes químicos:
Benzopirenos, nitrosaminas, nitritos, metales pesados como Hg o Pb. Percival Plott detectó un tipo de cáncer en los desollinadores, ello debido a un componente quimico del hollín.Agentes físicos:
Radiaciones ionizantes, radiación cósmica, UVA.Agentes biológicos:
Virus del papiloma humano, helycobacter pylori.Características de las células cancerígenas
1. Liberan factores de crecimiento por vía endocrina o paracrina.
2. Inducen la angiogénesis.
3. Omiten la apoptosis.
4. Invaden tejidos por metástasis.
5. No necesitan oxígeno, pero sí nutrientes.
6. No tienen capacidad de diferenciación.
2. Inducen la angiogénesis.
3. Omiten la apoptosis.
4. Invaden tejidos por metástasis.
5. No necesitan oxígeno, pero sí nutrientes.
6. No tienen capacidad de diferenciación.
Cáncer
El cáncer tiene un punto en común: Comienza con la falta de regulación del ciclo celular y además produce procesos en los que la célula a pesar de los daños producidos, generalmetne sobrevive.
En una región mamaria, una proliferación excesiva que diera lugar a un tumor benigno no tendría por qué ser un problema. Pero si la proliferación se extiendera a otros tejidos mediante metástasis estaríamos ante un proceso cancerígeno grave.
Las células aun cancerígenas necesitan alimentos para que no se produzca desnutrición celular, por lo que es común que se expresen factores de crecimiento de vasos sanguíneos en loque se coneoce como angiogénesis para hacer llegar nutrientes. Las células cancerígenas NO NECESITAN OXÍGENO, pero SÍ NECESITAN NUTRIENTES por lo que liberan el factor necesario para la angiogénesis. Además de aporte nutricional, los vasos sanguíneos sirven como medio para invadir otros tejidos mediante metástasis.
Una de las preguntas más frecuentes es por qué nuestro sistema inmunóligo no responde a las células tumorales. Pues bien, esto se debe a que estas poseen mecanismos que las hacen ser "invisibles" ante este.
El cáncer es una enfermedad genética, pues se producen modificaciones de ADN, aunque no tieene nada que ver con enfermedades hereditarias. Solo una pequeña población de cánceres es hereditaria, aquella que se transmite mediante las células gaméticas.
Características de las células tumorales:
1. Sin factores de crecimiento proliferan (al contrario que las células normales).
2.Liberan factres de crecimiento de carácter endrocrino o paracrino.
3.No se produce diferenciación celular.
4. Invaden tejidos por metástasis.
5.Promueven la angiogénesis
lunes, 14 de enero de 2013
La solubilida de un gas es proporcional a la presión ejercida por dicho gas
c(mol/l): k*P(atm)
Cuando se almacena un gas se hace a una determinada presión para que contenga disuelto todo el gas posible. Cuando varía esta presión al abrir la botella, disminuye la solubilidad del gas,ya que el liquido vuelve a estar a la presión atosférica y se evapora.
Efecto salino
El efecto salino consiste en que las interacciones iónicas hacen que las acrividades de los iones sean menores quessu concentraciones estequiométricas y la solubilidad aumenta.
Osmosis
Osmosis: Se produce un flujo neto a través de una membrana semipermeable desde la dislución más diluida a la más concentrada.
Osmosis inversa: Si se aplica presión sobre la disolución concentrada se pbliga a las moléculas a pasar a la más diluida. Se uitliza par aobtener agua potable desde agua salada.
Presión de vapor en las disoluciones y Ley de Raoult
Cuando las moléculas se evaporan en un recipiente, la presión del vapor es lo suficientemente alta para que las moléculas del vapor vuelvan al líquido, por lo que se establece un equilibrio constante. Todo líquido a una cierta temperatura puede establecer un equilibrio dinámico entre lasmoléculas que pasan del líquido al vapor y del vapor al líquido.
La presión de vapor es la presión ejercida por el líquido evaporado a depterminada temperatura. Por lo tanto hay una dependencia entre la temperatura y el tipo de líquido. Además;presión de vapor=punto de ebullición
*Ley de Raoult: Un soluto NO volátil disuelto disminuye la presión de vapor del disolvente (Pa0): Para conocer la presión de vapor del disolvente, la presión ejercida por el líquido (disolvente) debe ser multiplicada por la fracción molar para conocer verdaderamente la presión del disolvente y no la del soluto, que no se incluye en la presión de vapor.
Si tenemos dos líquidos, cada uno va a ejercer su propia presión. En caso de que el soluto sea volátil la presión de vapor va a ser la suma de las presiones parciales de cada uno de los componentes.Pt:Pa+Pb=xa·Pa+xb·Pb
*Las disoluciones IDEALES siempre cumplen la ley de Raoult.
*Las disoluciones NO ideales sólo la cumplen si son muy diluidas (xb<0,02)
Se puede representar cómo varían las presiones de vapor dependiendo de la composición (a una temp constante):
Fuerzas de cohesión>fuerzas de adhesión, las moléculas están más retenidas entre sí, y menos por el disolvente, así que la desviación es positiva.
Fuerzas de adhesión>fuerzas de cohesión, las moléculas están más retenidas por el disolvente, la volatilización es más difícil, así que la curva es negativa.
Cuando la presión de vapor=presión atmosférica el líquido hierve, por lo que se puede representar cómo varía el punto de ebullición a una determinada temp.
Así, podemos representar 2 cosas:
En el caso dos, la zona entre el líquido y el vapor es donde coexiste las dos fases, que de tratarse de una mezcla es muy inestable y nunca se puede permanecer en ella.
- Variación de la presión de vapor dependiendo de la composición (fuerzas adhesivas y cohesivas)
- Punto de ebullición a determinada temp.
Si seguimos la línea superior, el vapor se enriquece en el componente más volátil, mientras que en el líquido (línea inferior) queda el componente menos volátil. Esto a través de separaciones sucesivas nos permitirá lograr una pureza total en la consecución de todo el componente más volátil en una parte y todo el componente menos volátil en otra. Es el principio de la destilación.
Recuerda: Interacciones en disolución
En una disolución, se separan primeramente las moléculas del disolvente (AHa<0) y en segundo lugar las del soluto (AHb<0). A continuación interacionan las moléculas de soluto y disolvente (AHc>0). La entalpía total viene determinada por:
AHsol=AHa +AHb + AHc
Si las fuerzas entre los componentes son similares, practicamente no ha variación de energía al producirse la disolución de los compuestos. Este es el caso de las disoluciones ideales.
AHsol = 0 (aprox)
AHa+AHb= -AHc
Si las fuerzas de cohesión<fuerzas de adhesión el proceso de adhesión es exotérmico.
AHa+AHb<AHc AHsol<0
Si las fuerzas de cohesión>fuerzas de adhesión el proceso de adhesión es endotérmico.
AHa+AHb>AHc AHsol>0
Si fuerzas de cohesión>>>fuerzas de adhesión, el proceso es muy endotérmico y no se produce la disolución pues no hay suficiente energía así que se obtienen mezclas heterogéneas.
domingo, 13 de enero de 2013
El enlace químico
Entre
1916-19, G. N. Lewis, I. Langmuir y W. Kossel formularon
una propuesta sobre el enlace químico: Teoría de Lewis
• Los
electrones de valencia juegan un papel fundamental en el enlace
químico.
• La
transferencia de electrones conduce a los enlaces iónicos.
• La
compartición de electrones lleva a los enlaces covalentes
(introducido por Langmuir).
• Los
electrones se transfieren o se comparten de manera que los
átomos adquieren una configuración de gas noble: octeto.
Estructuras
de Lewis.
Lewis
desarrolló un conjunto de símbolos para su teoría.
Un
símbolo de Lewis consiste en un símbolo químico que
representa el núcleo y los electrones internos de un
átomo y unos puntos situados alrededor del símbolo
representan los electrones de valencia o electrones más
externos.
El
enlace entre un átomo de hidrógeno y un átomo de cloro implica
la compartición de electrones. Esta compartición da lugar a un
enlace covalente.
• Los
círculos de trazos representan las capas electrónicas externas
de los átomos enlazantes.
•El
número de puntos que hay sobre cada circunferencia representa el
número efectivo de electrones de cada capa de valencia.
• Los
electrones compartidos los contamos dos veces, ese par de electrones
compartidos constituye el enlace covalente.
Regla
del octeto
Para
formar una estructura de Lewis es requisito tener ocho electrones
en la capa de valencia para cada. No obstante, el átomo de H es
una excepción a esta regla porque sólo puede tener dos
electrones en la capa de valencia.
La
compartición de un par de electrones entre átomos enlazados da
lugar a un enlace covalente simple.
Enlaces
covalentes coordinados
Un
enlace covalente en el que uno de los átomos
contribuye con ambos electrones del par compartido
se denomina un enlace covalente coordinado.
No
se puede distinguir entre un enlace covalente coordinado y uno
normal.
Enlaces
covalentes múltiples
Los
átomos enlazados comparten entre sí dos o tres pares de
electrones, constituyendo un
enlace covalente doble o triple (múltiple).
Polaridad
y electronegatividad
Enlace
covalente polar: aquel en el
que dos átomos no comparten por igual los electrones. En
estos enlaces, los electrones se desplazan hacia el elemento de
mayor carácter no metálico.
Se
puede representar mediante una estructura de Lewis en la que el par
de electrones enlazante está más próximo al Cl que al H.
Se
dice que hay una separación de carga con una carga parcial
positiva (δ+) sobre el H y una carga parcial negativa (δ-) sobre
el Cl.
Electronegatividad
(EN)
Describe
la capacidad que tiene un átomo para competir por los electrones con
otros átomos a los que está unido.
La
electronegatividad está relacionada con la Energía de
Ionización (I) y la afinidad
electrónica (AE).
Una
escala de electronegatividad muy utilizada fue diseñada por
Pauling:
*Los
valores van desde 0,7 (Cs y Fr) hasta 4,0 (F).
*Cuanto
más pequeño es el valor de EN, más metálico es el elemento.
*Cuanto
más grande es el valor de EN, menos metálico es el elemento.
A
partir de la diferencia de electronegatividad (ΔEN),
que es la diferencia en valor absoluto de EN de los átomos
enlazados describir la polaridad de un enlace covalente.
-Si
ΔEN es muy pequeño, el
enlace es esencialmente covalente.
-Si
ΔEN es grande, el
enlace es esencialmente iónico.
-Para
valores intermedios de ΔEN, el
enlace se considera covalente polar.
Escritura
de las estructuras de Lewis
Hay
que tener en cuenta:
-Todos
los electrones de valencia
de los átomos de una estructura de Lewis deben
aparecer en ella.
-Generalmente,
todos los electrones están apareados.
-Generalmente,
cada átomo requiere un octeto
(excepto el H).
-Algunas
veces son necesarios enlaces covalentes múltiples.
-Los
átomos C, N, O, P y S son los que más fácilmente forman
enlaces covalentes múltiples.
Cargas
formales (CF)
Son
cargas aparentes que aparecen sobre algunos átomos de una estructura
de Lewis cuando los átomos no han contribuido con igual número de
electrones al enlace covalente que los une.
Es
el número de electrones de valencia en el átomo menos el
número de e asignados a ese átomo en la estructura de Lewis.
*Los
e de los pares solitarios se cuentan como pertenecientes por
completo al átomo en que se encuentran.
*Los
e de los pares de enlace se dividen por igual entre los átomos
enlazados.
- CF = e de valencia en el átomo libre – e del par solitario – (e de enlace)/2
Reglas
generales para ver si una estructura es aceptable:
1.
La suma de las cargas formales es igual a la carga total de la
molécula o el ion.
2.
Si son necesarias cargas formales, éstas deben ser tan pequeñas
como sea posible.
3.
Las cargas formales negativa suelen aparecer en los
átomos más electronegativos y las positivas en los átomos menos
electronegativos.
4.
Las cargas formales del mismo signo en átomos adyacentes son poco
probables.
- Comenzamos por el esqueleto de la estructura:
Distinguir
entre los átomos centrales y los átomos terminales.
• Los
átomos de H son siempre átomos terminales.
• Los
átomos centrales suelen ser los de menor electronegatividad.
• Los
átomos de C son casi siempre átomos centrales. Ésta es una
característica común de moléculas orgánicas.
•Con
la excepción de moléculas orgánicas en forma de cadena, las
moléculas e iones poliatómicos tienen estructuras que suelen
ser compactas y simétricas.
Excepciones
a la regla del octeto
*Especies
con número impar de electrones (radicales):
*Octetos
incompletos:
Excepciones
a la regla del octeto
*Octetos
expandidos: Las estructuras
suelen estar formadas por átomos no metálicos situados a partir
del tercer periodo: P y S son muy comunes.
Tras
llenar las subcapas 3s y 3p del átomo central, los
electrones ocupan la subcapa vacía 3d.
Método
de la resonancia
El
oxígeno se presenta normalmente como molécula diatómica pero
también puede presentarse como molécula triatómica de ozono, O3.
Las
dos estructuras de Lewis presentan un enlace sencillo y uno doble, y
la evidencia experimental indica que ambos enlaces son
iguales, con una distancia intermedia entre el enlace doble y
sencillo, por lo que se dice que existe resonancia.
Se puede decir que los enlaces del ozono son
intermedios entre sencillos y dobles, es decir, enlaces 1,5.
La
verdadera estructura de Lewis no es ninguna de las dos sino un
híbrido de resonancia de las dos estructuras contribuyentes.
Geometría
molecular: modelo RPECV
La
geometría molecular se basa en la figura geométrica que
resulta de unir con líneas rectas los núcleos enlazados.
Así, definimos:
Longitudes
de enlace: distancias entre los
núcleos.
Ángulos
de enlace: ángulos entre
líneas adyacentes que representan los enlaces.
Teoría
RPECV (repulsión de pares de electrones de la capa de valencia):
• Los
pares de electrones se repelen entre sí, tanto si están en enlaces
químicos (pares enlazantes) como
si no están compartidos (pares solitarios).
Los pares de electrones se disponen alrededor de un
átomo con orientaciones que minimicen las repulsiones.
•
Geometría
de grupos de electrones: distribución
de los pares de electrones.
•
Geometría
molecular: distribución de los
núcleos.
¿Cómo
aplicamos la teoría RPECV?
- Escriba una estructura de Lewis aceptable.
- Determine el número de grupos de electrones que hay alrededor del átomo central (A) y establezca si son grupos enlazantes (X) o pares solitarios (E).
- Los enlaces múltiples cuentan como un solo grupo de electrones.
- La notación será AXnEm.
- Establezca la geometría de grupos de electrones: lineal, trigonal-plana, tetraédrica, bipiramidal trigonal, octaédrica.
- Determine la geometría molecular.
Pares
solitarios y geometría molecular:
Los
pares de e solitarios se extienden más que los pares de e
enlazantes.
El
orden de mayor a menor de las fuerzas repulsivas es:
*par
solitario - par solitario
*par
solitario - par enlazante
*par
enlazante - par enlazante
Geometría
de los pares de e-
Lineal
E+X=2
Trigonal
plana X+E=3
Tetraédrica
X+E=4
Bipiramidal
plana X+E=5
Octaédrica
X+E=6
Geometría
molecular
Lineal
AX2
Piramidal
trigonal AX3
Tetraédrica
Balancín
AX4E
Forma
de T AX3E2
Lineal
AX2E3
Pirámide
cuadrada AX5E
Plano
cuadrada AX4E2
Hibridación
sp
sp2
sp3
sp3d
“
“
sp3d2
Forma
de las moléculas y momentos dipolares
En
la molécula de HCl, el átomo de Cl es más electronegativo que
el átomo de H, así que los electrones están desplazados hacia
el átomo de Cl.
La
molécula de HCl es una molécula polar y la magnitud del
desplazamiento de la carga en un enlace covalente polar viene
dado por el momento dipolar, μ, que es el producto de la carga
parcial por la distancia:
- μ = d·δ
Cuando
δ·q tiene un
valor de 3,34×10-30 culombio·metro, μ es
igual a 1 debye (D).
Moléculas
polares y no polares
Aunque
una molécula pueda tener enlaces polares, la suma puede ser cero. En
ese caso, la molécula no es polar, como en el caso del dióxido de
carbono.
Moléculas
polares μ ≠0
*Moléculas
diatómicas con enlace polar.
*Moléculas
poliatómicas que contienen enlaces polares/pares de e- libres
distribuidos de tal manera que no se cancelan.
Moléculas
apolares: μ =0
*Moléculas
diatómicas SIN enlace polar.
*Moléculas
poliatómicas que contienen enlaces polares/pares de e- libres que SE
ANULAN entre sí.
Orden
de enlace
Se
puede definir como el número de enlaces existentes entre dos átomos.
De
forma simple, un enlace simple, orden = 1, un enlace doble, orden = 2
y un enlace triple, orden = 3.
Cuanto
mayor es el orden de enlace, menor es la longitud de enlace y el
enlace es más fuerte.
De
acuerdo con las teorías cuánticas, el orden de enlace puede no ser
un número entero. Esto se debe a que según la teoría de los
orbitales moleculares, el orden de enlace se puede definir como el
resultado del siguiente cálculo: 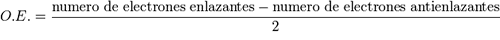
Se
forman OM enlazantes/antienlazantes a partir de orbitales atómicos.
Número
de orbitales moleculares (OM) = número de orbitales atómicos.
Los
electrones se colocan en los OM disponibles de energía más baja.
Se
cumple el principio de exclusión de Pauli y se sigue la regla de
Hund.
Las
especies estables tienen más electrones en los orbitales enlazantes
que en los antienlazantes.
Energía
de disociación del enlace
La
energía de disociación del enlace, D, es la cantidad de energía
necesaria para romper un mol de enlaces covalentes en una especie
gaseosa. Las unidades del SI son kJ/mol de enlaces.
Una
energía de enlace media es el valor medio de las energías de
disociación de enlace
de
varias especies distintas que tienen determinados enlaces.
Las
energías de enlace pueden servir para predecir si una
reacción será exotérmica (ΔH < 0) o endotérmica (ΔH >
0):
ΔH
= ∑energía de los enlaces formados - ∑energía de los enlaces
rotos
Teoría
del Enlace de Valencia
Cuando
se acercan dos átomos que inicialmente se encuentran muy alejados
uno de otro:
1.
Los electrones son atraídos por los dos núcleos.
2.
Los electrones se repelen unos a otros.
3.
Los dos núcleos se repelen entre sí.
Si
se representa la energía potencial en función de la distancia entre
los núcleos atómicos:
*Las
energías negativas corresponden a una fuerza atractiva
neta.
*Las
energías positivas corresponden a una fuerza repulsiva neta.
El
solapamiento de orbitales atómicos describe el enlace covalente.
El
área de solapamiento de los orbitales está en fase.
Se
trata de un modelo de enlace localizado.
Se
produce solapamiento entre los orbitales 1s del H y los
orbitales 3pz y 3px del S, quedando el orbital 3py con un par
de electrones sin compartir.
Hibridación
El
concepto del traslapo de los orbitales atómicos también se aplica a
moléculas poliatómicas. Sin embargo, un esquema satisfactorio del
enlace también debe explicar la geometría molecular.
Si
sólo se pudiesen utilizar orbitales p, los ángulos de enlace
serían siempre de 90°.
La
hibridación consiste en una operación matemática que combina
los orbitales atómicos para dar lugar a orbitales híbridos,
que están de acuerdo con la geometría molecular.
Los
cuatro orbitales de valencia del C se hibridan y se obtienen 4
orbitales híbridos sp3 degenerados.
Orbitales
híbridos: orbitales atómicos
que se obtienen cuando dos o más orbitales NO EQUIVALENTES se
combinan entre sí para prepararlos para la formación del enlace
covalente.
La
teoría de EV necesita conocer la geometría molecular de la
molécula. Normalmente se basa en la teoría RPECV.
El
proceso consiste en:
1.
Escribir una estructura de Lewis aceptable.
2.
Utilizar la teoría RPECV para predecir la geometría probable
de grupos de electrones.
3.
Seleccionar el esquema de hibridación correspondiente a
la geometría de grupos de electrones.
Teoría
de orbitales moleculares
La
teoría de enlace valencia es una de las dos propuestas de la
mecánica cuántica para explicar los enlaces en las moléculas.
Explica, al menos cualitativamente, la estabilidad del enlace
covalente en términos del traslapo de orbitales atómicos.
Utilizando el concepto de hibridación, la teoría de enlace valencia
puede explicar la geometría molecular predicha por el modelo RPECV.
Sin embargo, la suposición de que los electrones en una molécula
ocupan orbitales atómicos de los átomos individuales, es sólo una
aproximación, ya que cada electrón enlazante en una molécula debe
estar en un orbital característico de la molécula como un todo. En
algunos casos la teoría de enlace valencia no explica
satisfactoriamente algunas de las propiedades observadas de las
moléculas. Podemos resumir en que la TEV explica aspectos
cuantitativos, la forma de la molécula, pero la TOM explica aspectos
cuantitativos, referentes a la energía.
Los
orbitales atómicos están aislados en los átomos.
Los
orbitales moleculares abarcan dos o más átomos.
Se
expresan como combinación lineal de orbitales atómicos:
Un
orbital molecular de antienlace tiene mayor energía y menor
estabilidad que los orbitales atómicos que lo formaron. Como lo
indican los nombres de “enlace” y “antienlace”, el acomodo de
electrones en un orbital molecular de enlace produce un enlace
covalente estable, en tanto que el acomodo de electrones en un
orbital molecular de antienlace produce un enlace inestable.
En
los orbitales moleculares de enlace, la densidad electrónica es
máxima entre los núcleos de los átomos que se enlazan. Por otra
parte, en los orbitales moleculares de antienlace la densidad
electrónica disminuye hasta cero entre los dos núcleos.
El
enlace σ
es
un enlace que se forma entre dos átomos de un compuesto covalente,
debido a la superposición directa o frontal de los orbitales; es más
fuerte y determina la geometría de la molécula.
Traslapo frontal.
El enlace Π que se forma después del enlace sigma; es el segundo o tercer enlace formado entre dos átomos, debido a la superposición lateral de los orbitales “p”. Sus electrones se encuentran en constante movimiento. Traslapo lateral.
El enlace Π que se forma después del enlace sigma; es el segundo o tercer enlace formado entre dos átomos, debido a la superposición lateral de los orbitales “p”. Sus electrones se encuentran en constante movimiento. Traslapo lateral.
¿CÓMO EXPLICA LA TEORIA DE ENLACE VALENCIA LOS ENLACES SENCILLOS, DOBLES Y TRIPLES?
Un
enlace sencillo es el resultado del solapamiento de orbitales a lo
largo del eje internuclear (línea imaginaria que une los dos
núcleos). Este enlace se conoce como enlace sigma, y se obtiene del
pareamiento de electrones debido al solapamiento de dos orbitales
"s", o de un orbital "s" con un orbital Px, o de
dos orbitales Px, o de cualesquiera dos orbitales atómicos que se
solapen a lo largo del eje internuclear (eje de X).
En un enlace pi se requiere del solapamiento de orbitales que interaccionen fuera del eje internuclear, específicamente orbitales 'Py' y/o 'Pz' , que quedan perpendiculares al eje internuclear (eje de X).
En un doble y triple enlace, además del enlace sigma, se requiere de uno o dos enlaces pi, respectivamente.
¿COMO EXPLICA LA TEORIA DE ORBITALES MOLECULARES LOS ENLACES SENCILLOS, DOBLES Y TRIPLES?
Por la teoría de orbitales moleculares se entiende que el solapamiento de los orbitales a lo largo del eje internuclear genera un orbital de enlace llamado sigma . Por lo tanto, todo enlace sigma implica un enlace sencillo y viceversa. En cada enlace sigma hay dos electrones pareados. Su densidad electrónica es cilindricamente simétrica alrededor del eje internuclear.
Para el caso de enlaces dobles o triples, la teoría de orbitales moleculares especifíca la formación de un orbital sigma y un orbital "pi" para un doble enlace y de un orbital sigma y dos orbitales "pi" para el triple enlace.
Un orbital "pi" se genera por el solapamiento de los orbitales que interaccionan fuera del eje internuclear: por lo general, orbitales atómicos ''p''. Su densidad electrónica se ubica sobre y debajo de este eje. Cada orbital posee un par de electrones pareados: en este caso se produce un enlace pi.
(Sólo se indican los orbitales de enlace; por conveniencia los orbitales de antienlace no se ilustran. Los dos lóbulos que constituyen el orbital molecular pi de enlace forman un sólo enlace).
La teoría de orbitales moleculares es muy conveniente para explicar el fenómeno de la deslocalización de electrones: electrones que pueden enlazar más de dos átomos a la vez debido a que se encuentran en orbitales moleculares deslocalizados, es decir, solapados y abarcando varios átomos.
Si
el átomo central forma dobles enlaces, tendrá hibridación sp2. Si
forma un triple enlace, tendrá hibridación sp.
Reacciones químicas
1. Reacción
química. Estequiometría
La
reacción química es un proceso en el que un conjunto de sustancias
llamadas reactivos se transforma en un nuevo conjunto de sustancias
denominadas productos.
La
ecuación química es una notación simbólica o abreviada que
representa a la reacción química: R P
Se
debe cumplir que todos los átomos que constituyen los
reactivos están presentes y en la misma proporción en los
productos: las reacciones deben esta
r ajustadas.
Coeficientes
estequiométricos: Coeficientes necesarios para ajustar una
ecuación química.
Para
ajustar ecuaciones:
1.
Ajustar en primer lugar los elementos que aparecen solamente
en un compuesto en cada lado.
2.
Ajustar en último lugar los elementos libres.
3.
En algunas reacciones hay grupos de átomos que no se modifican. En
estos casos, ajuste los grupos como si se tratase de una unidad.
4.
Se pueden utilizar coeficientes fraccionarios, que se eliminan al
final multiplicando.
En
algunos casos hay que indicar la forma física de reactivos y
productos. Esta información suele aportarse entre paréntesis
y los símbolos que se suelen emplear son: g(gas), l(líquido),
s(sólido) y aq(disolución acuosa)
En
otras ocasiones se indican las condiciones de reacción encima o
debajo de la flecha de la ecuación. P. ej., la letra griega Δ
indica calentamiento de la mezcla de la reacción.
La
estequiometría incluye todas las relaciones cuantitativas en
las que intervienen:
• Las
masas moleculares y atómicas.
• Las
fórmulas químicas.
• Una
relación de moles, obtenida partir de la ecuación química.
Hay
que incluir factores de conversión adicionales teniendo en cuenta
el volumen, la densidad y la composición porcentual, concentración,
etc.
Determinación
del reactivo limitante
Proporciones
estequiométricas: Cuando todos los reactivos se consumen de
manera completa y simultánea.
Reactivo
limitante: aquel que se consume completamente.
El reactivo que se consume completamente determina las cantidades de
los productos formados.
La
forma más fácil es pensar cuantos moles te hacen falta para que el
reactivo se gaste. Si la cantidad que tienes es mayor, entonces el
reactivo limitante es el otro.
En
muchos casos, la reacción sucede en varias reacciones consecutivas:
4 NH3 (g) + 5 O2
(g) 4 NO (g) + 6 H2O (g)
2 NO (g) + O2 (g) 2
NO2 (g)
3 NO2 (g) + H2O (l)
2 HNO3(aq) + NO (g)
Generalmente,
se pueden combinar en una única ecuación neta:
12
NH3 + 21 O2 8 HNO3 + 4 NO + 14 H2O
Las
sustancias que se producen en una etapa y se consumen en otra etapa
posterior se denominan intermedios de reacción.
A veces se producen reacciones simultáneas, cuando dos o
más sustancias reaccionan independientemente pero a la vez.
Rendimiento
de una reacción
El
rendimiento teórico es la cantidad de producto que se
obtendrá si reacciona todo el reactivo limitante.
El
rendimiento real es la cantidad real de producto obtenida.
El
% de rendimiento (o rendimiento
porcentual)
se define: % de rendimiento =
·100
Cuando
% de rendimiento es 100%, se dice que la reacción es cuantitativa.
El
% de rendimiento suele ser menor del 100% debido a reacciones
secundarias, que forman otros subproductos, problemas en la
purificación o el aislamiento de los productos, reacciones
reversibles, etc.
2.
Reacciones en disoluciones acuosas
• El
agua es el disolvente más común, disuelve a numerosas sustancias.
• Los
solutos que se disocian en iones se denominan electrolitos.
•
Pueden ser electrolitos
fuertes, cuando la disociación es completa.
MgCl2(s)
Mg2+ (aq) + 2 Cl- (aq)
• O
electrolitos débiles, cuando sólo lo hacen parcialmente.
• Los
solutos que no se disocian en iones se denominan no electrolitos.
Fuente
de electricidad
En
general, todos los compuestos iónicos solubles y sólo unos
pocos compuestos moleculares son electrolitos fuertes.
La
mayoría de los compuestos moleculares son, o no electrolitos o
electrolitos débiles.
3.
Reacciones ácido-base
•
Inicialmente, usaremos la
teoría ácido-base de Arrhenius (1884) para la definición de
ácidos y bases:
• Los
ácidos proporcionan H+ en disolución acuosa.
o
Ácidos fuertes (se ionizan completamente en disolución).
o
Ácidos débiles (se ionizan de forma parcial en disolución).
• Los
ácidos contienen átomos de hidrógeno que pueden ionizarse.
• Las
bases proporcionan OH– en disolución acuosa.
*Bases
fuertes (se disocian por completo o casi, hidróxidos del grupo 1 y
algunos del grupo 2).
*Bases
débiles (determinadas sustancias producen iones al reaccionar con
agua y no simplemente disolviéndose en ella):
(p.
ej. NH3 + H2O NH4+ + OH- )
• Las
bases contienen iones OH combinados con iones metálicos (KOH) o son
identificadas mediante ecuaciones químicas.
Na2CO3 (s) +
H2O(l)→ HCO3- (aq) + 2 Na+ (aq) + OH- (aq)
6.
Reacciones de oxidación-reducción
Oxidación:
El estado de oxidación de algún elemento aumenta en la reacción.
Reducción:
El estado de oxidación de algún elemento disminuye en la
reacción.
La
oxidación y la reducción siempre se producen de forma conjunta.
Fe2O3 (s) + 3 CO2(g)
2 Fe(l) + 3 CO2 (g)
Un
agente oxidante (un oxidante): Contiene un elemento cuyo
estado de oxidación disminuye en la reacción redox.
Un
agente reductor (un reductor): Contiene un elemento cuyo
estado de oxidación aumenta en la reacción redox.
En
las reacciones de desproporción (o dismutación), un mismo
compuesto se reduce y se oxida. 2 H2O2 2 H2O+O2
*Ajuste
de las reacciones de oxidación-reducción
-Método
de la semirreacción (ión-electrón).
1.
Determinar los estados de oxidación.
2.
Escribir las ecuaciones para las semirreacciones.
3.
Ajustar todos los átomos excepto los que no sean ni de H ni de O.
4.
Ajustar el oxígeno utilizando H2O.
5.
Ajustar el hidrógeno utilizando H+ (ajuste en medio ácido).
6.
Ajustar la carga utilizando e-.
7.
Sumar las semirreacciones para eliminar los electrones.
8.
Añadir contraiones si son necesarios.
-Para
ajustar en medio básico:
1.
Tratar la ecuación como si fuese en medio ácido.
2.
Se añaden a cada lado de la ecuación tantos OH- como H+ haya.
3.
Los OH- y H+ se neutralizan formando H2O.
4.
Eliminar el H2O en exceso.
5.
Reacciones de precipitación
Los
iones solubles se pueden combinar para formar un compuesto insoluble,
que precipita.
Ag+
(aq) + Cl- (aq) AgCl(s)
Cuando
dos compuestos iónicos forman un precipitado sólido, se produce un
intercambio de iones.
Ej.
KBr (aq) + AgNO3 (aq)
Se
forman compuestos de coordinación: un anión o catión
poliatómico compuesto por un ion metálico central y ligandos.
AgCl(s) +
2 NH3(aq) [Ag(NH3)2]+ (aq) + Cl- (aq)
Suscribirse a:
Entradas (Atom)